一文看懂 中美藥品專利鏈接制度及藥企應(yīng)對策略

藥品專利鏈接制度源于美國,1984年,美國通過了《藥物價格競爭和專利期恢復(fù)法案》(又稱為Hatch-Waxman法案),包括藥品專利鏈接制度、藥品專利保護期補償、Bolar例外、數(shù)據(jù)保護等幾個方面,建立了一套完整藥品知識產(chǎn)權(quán)法律制度,明確了原研藥企業(yè)和仿制藥企業(yè)利益博弈的規(guī)則。
專利聲明制度
Hatch-Waxman法案構(gòu)建了一套簡化仿制藥上市的程序,來確保創(chuàng)新藥專利期屆滿后仿制藥能夠盡快上市,即仿制藥簡化申請(Abbreviated New Drug Application ,ANDA)制度。仿制藥上市申報時只需要提供證據(jù)證明:生產(chǎn)的仿制藥與經(jīng)過批準(zhǔn)的原研藥具有生物與藥理上的等效性;生產(chǎn)的仿制藥與經(jīng)過批準(zhǔn)的藥品在該仿制藥藥品標(biāo)簽表明的推薦使用狀態(tài)下具有相同的安全性與有效性。
專利挑戰(zhàn)制度
仿制藥申請人在作出第IV段聲明時,即啟動了專利挑戰(zhàn)程序。在該程序中專利挑戰(zhàn)人具有及時告知義務(wù),即在受理后的20天內(nèi)將專利挑戰(zhàn)通知專利權(quán)人或新藥持有人,并且就專利無效或不侵權(quán)的事實和法律依據(jù)進行說明。
在法院判定仿制藥侵犯專利權(quán)時,仿制藥需要等到專利過期之后才能獲得上市許可。如果在30個月內(nèi)專利期屆滿或法庭作出不侵權(quán)的裁決,并且符合審批要求,則ANDA上市的批準(zhǔn)生效。如果30個月后專利糾紛仍未解決,F(xiàn)DA可對ANDA申請人頒發(fā)臨時性許可批件,但ANDA申請人需承擔(dān)上市銷售后侵犯專利權(quán)法律責(zé)任的風(fēng)險。
首仿藥市場獨占期制度
為促進仿制藥挑戰(zhàn)原研藥專利,Hatch-Waxman法案規(guī)定第一家通過專利挑戰(zhàn)并獲得上市審批的ANDA申請人獲得180天的市場獨占期,在這180天內(nèi),F(xiàn)DA不會批準(zhǔn)其他仿制藥上市。
我國藥品專利鏈接制度,第四次修訂后的《專利法》第76條規(guī)定:“藥品上市審評審批過程中,藥品上市許可申請人與有關(guān)專利權(quán)人或者利害關(guān)系人,因申請注冊的藥品相關(guān)的專利權(quán)產(chǎn)生糾紛的,相關(guān)當(dāng)事人可以向人民法院起訴,請求就申請注冊的藥品相關(guān)技術(shù)方案是否落入他人藥品專利權(quán)保護范圍作出判決。藥品上市許可申請人與有關(guān)專利權(quán)人或者利害關(guān)系人也可以就申請注冊的藥品相關(guān)的專利權(quán)糾紛,向?qū)@姓块T請求行政裁決。”
藥品專利鏈接制度的具體規(guī)則:
1、建立專利信息登記平臺
2、明確藥品專利信息登記范圍
3、規(guī)定仿制藥申請人專利狀態(tài)聲明制度
4、明確專利權(quán)人或者利害關(guān)系人提出異議的時限
5、對化學(xué)藥品設(shè)置審評審批等待期
6、對藥品審評審批實施分類處理
7、對仿制藥專利挑戰(zhàn)進行鼓勵
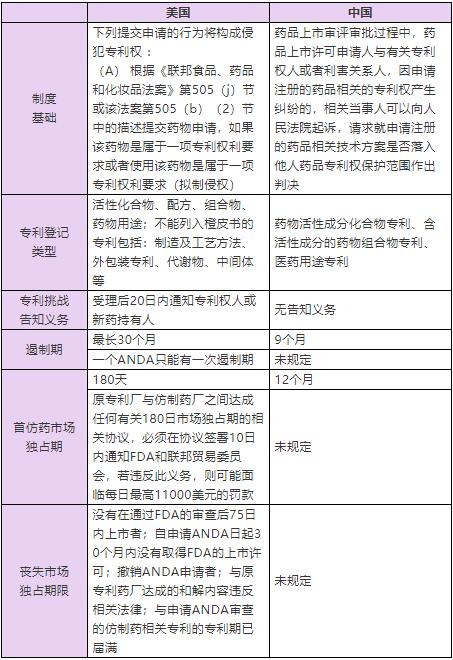
中美藥品專利鏈接制度差異性對比
1. 原研藥企業(yè)應(yīng)對策略:
原研藥企業(yè)首先應(yīng)關(guān)注中國上市藥品專利信息登記平臺對原研藥的規(guī)定,目前鏈接制度尚未明確《中國上市藥品目錄集》、中國上市藥品專利信息登記平臺兩個系統(tǒng)的銜接方式,需要關(guān)注相關(guān)配套措施,及時登記藥品及專利信息。
做好高價值專利布局,構(gòu)建嚴(yán)密高效的專利保護網(wǎng),最終形成對企業(yè)有利格局的專利組合。藥品專利早期解決機制的訴由對權(quán)利要求的質(zhì)量提出了更高的要求,原研藥企業(yè)保護范圍合理且穩(wěn)定的高質(zhì)量專利才是遏制仿制藥上市時的基石。
建立預(yù)警與防控機制,定期關(guān)注中國上市藥品專利信息登記平臺。在我國,仿制藥申請人只需在平臺上登記,對相關(guān)專利權(quán)人或藥品持有人沒有告知義務(wù),所以相關(guān)專利權(quán)人或藥品持有人需要持續(xù)關(guān)注登記平臺并對平臺上的登記信息進行侵權(quán)與否的初步判斷。
在確定仿制藥侵權(quán)時,應(yīng)及時按照藥品專利糾紛早期爭議解決機制,提起訴訟及行政裁決申請,阻礙仿制藥上市。
原研藥企應(yīng)積極維權(quán),及時開展侵權(quán)情況的調(diào)查,若確定仿制藥企業(yè)存在銷售或許諾銷售行為,原研藥企應(yīng)及時保全證據(jù),在侵權(quán)行為地或被告所在地提起專利侵權(quán)訴訟。
仿制藥企業(yè)應(yīng)對策略:
在研發(fā)立項前,做好充分的信息調(diào)研準(zhǔn)備工作,討論是否開展項目研究工作。前期調(diào)研不但應(yīng)當(dāng)關(guān)注專利侵權(quán)的風(fēng)險,還應(yīng)當(dāng)進行藥品注冊信息、臨床信息、實驗技術(shù)分析和市場分析等方面的內(nèi)容。當(dāng)然,專利侵權(quán)風(fēng)險評估是最為重要的環(huán)節(jié)之一,仿制藥企業(yè)應(yīng)核查現(xiàn)行有效的專利,同時還應(yīng)當(dāng)考慮和分析其他未授權(quán)專利,確定這些專利的授權(quán)是否會對產(chǎn)品上市構(gòu)成障礙。
在上市審批過程中遇到原研藥企發(fā)起的專利訴訟或裁定申請,應(yīng)當(dāng)要積極應(yīng)對,可以采取現(xiàn)有技術(shù)抗辯,具有不視為專利侵權(quán)的法定情形抗辯,或者徑直對涉案專利提起無效宣告。
仿制藥專利挑戰(zhàn)成功后,在12個月內(nèi)不再批準(zhǔn)其他相同品種的化學(xué)仿制藥上市,因此仿制藥企業(yè)通過專利挑戰(zhàn)并取得首仿藥資格上市,可為企業(yè)贏得獨占市場。
隨著藥品專利鏈接制度的實施,樂知網(wǎng)小編預(yù)計藥品專利糾紛會快速增長,也對企業(yè)的專利工作提出了更高的要求。無論是原研藥企業(yè)還是仿制藥企業(yè),都需加強專利的保護。
關(guān)鍵詞: 專利侵權(quán) 專利 ?